CLEM(相关光和电子显微镜)和LMD - 快速,精确地跟踪标记结构
在细胞生物学中蛋白质和细胞器调查的增加有时需要不同的成像方法的组合。这克莱姆特别是耦合技术的方法,例如光和电子显微镜。关键目标是在电子显微镜水平下用光学显微镜进行以透光器获得的图像,即用超微结构和3D信息将动态事件相关联。使用LMD.,可以在培养基衬底的表面上产生参考坐标的系统,以在样品制备期间能够在标记细节的快速和精确的位置。该过程在图1中令人印象深刻地说明。
图。图1:印迹到细胞培养基质上的参考网格。(a)激光微探针参考网格的方案。使用激发滤光器BP 545/30(b),BP 480/40(c)和BP 360/40(d),在离浊度显微镜下成像图案化的aclar衬底。网格荧光比GFP.标记蛋白的信号。(e)参考网格在BrightField中可见,并通过扫描电子显微镜(F)。(g-i)由于炭黑的熔化,正如扫描所示的压印正和负图案em.(G)。结果,在聚合之后,除去培养基底物(H),该图案表现为负和正标记,留下可见孔(I)em.部分。(j)安装在镀金直播电池载体上的预图案衬底的图片[1]。
Nanosims - 第三维的结构
图2:用激光微粉切割滤波器标记(LMD.)催化记者沉积系统(卡) -鱼纳米级二次离子MS(纳米末端)在相同的过滤器位置分析。小盒子照片显示纳米斯米斯的图像13.C-掺入的细胞(红色)覆盖在卡上 -鱼用于检测古细胞的图像。每个网格的大小约为50×50μm,标有约50×50μmLMD.系统[2]。
LMD在Live Cell Research中 - 一种“蓄意破坏”的方法
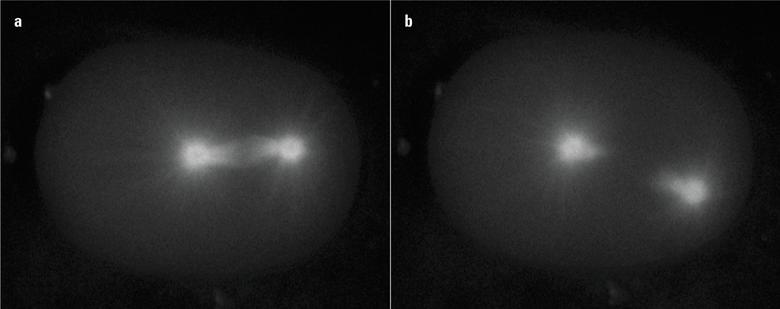
徕卡LMD.在活细胞部门中特别有用,用于故意机械破坏细胞结构,例如Centrosomes,微管和膜。例如,通过激光器可以穿孔细胞膜以允许先前被膜完全阻挡的物质渗透,根据Monica教授得从遗传医学系,日内瓦大学发展。最重要的是,可以在细胞分割期间操纵细胞的主轴装置(图3)。
图3:野生型单细胞胚胎中的有丝分泌纺锤体消融。一种C. Elegans.表达α-小蛋白融合的单细胞胚胎GFP.。在(a)之前和激光烧蚀(b)之前的有丝分裂主轴。两个主轴杆在消融后分开[5]。
参考
- Spiegelhalter C,Tosch V,Hentsch D,Koch M,Kessler P,Schwab Y和Laporte J:从动态活细胞成像到3D超微结构:高压冷冻和相关光 - 电子显微镜的新型集成方法。PLOS一个5(2):E9014(2010);DOI:10.1371 / journal.pone.0009014。
- Morono Y,Terada T,Nishizawa M,ITO M,Hillion F,Takahata N,Sano Y和Inagaki F:深层外部面板微生物细胞中的碳和氮素同化。PNA 108(45):18295-300(2011)。
- Thompson AW,Foster Ra,Krupke A,Carter Bj,Musat N,Vaulot D,Kuypers MMM和Zehr JP:单细胞蓝藻与单细胞真核藻类共生。科学337(6101):1546-50(2012);DOI:10.1126 / Science.1222700。
- Polerecky L,Adam B,Milucka J,Musat N,Vagner T和Kuypers MMM:看@ nanosims - 一种分析环境微生物学中纳米米数据的工具。环境微生物学14(4):1009-23(2012)。
- Grill SW,GönczyP,Stelzer EHK和Hyman AA:极性控制在Caenorhabditis elefars胚胎中控制不对称主轴定位的力量。自然409:630-33(2001);DOI:10.1038 / 35054572。