神经元网络中的分子动力学
神经系统学习和响应环境的能力反映了神经元的潜在能力,以动态改变其连接的数量,类型和优势。这些称为突触的连接是突触后神经元和突触前终端之间的高度有组织的接触位点。188金宝搏的网址专用突触膜含有各种各样的分子,如受体,离子通道和相关的结构蛋白,其精确的亚细胞组织有助于其适当的功能。大量研究提供了证据表明这些蛋白质的位置及其相对于突触的位置基本上影响其功能作用。本地递质的神经递质受体局部地直接暴露于神经元的突触后隔室的突触膜,直接暴露于释放的神经递质。
因此,它们以一种短暂的方式被激活,产生快速的突触后反应,这些反应精确地锁定在突触前动作电位上。相反,位于突触外质膜的受体,远离突触部位,被溢出的神经递质激活,产生一种紧张性传导,这种传导并不精确地锁定在单个突触前动作电位上,而是在较慢的时间尺度上反映整个神经网络的活动[1].受体也可以位于突触前,要么位于轴突终末的突触外膜上,要么位于突触前网格上,在那里它们被同一或相邻的钮扣释放的神经递质激活。与神经递质受体一样,离子通道也定位于神经元的躯体树突膜和轴突末端。突触后通道通常参与突触输入的整合和可塑性,以及通过介导缓慢抑制性突触反应和促进静息膜电位来控制神经元兴奋。
突触前通道集中于神经元的突触前活跃区或位于神经元的突触外膜,参与调节神经递质的释放,从而在神经元活动的突触前调节中发挥作用。因此,不难理解,当同一受体和离子通道针对不同的细胞亚细胞室时,可以满足非常不同的功能要求[1].
此外,膜蛋白激活对突触整合和递质释放调控的影响,主要取决于靶神经元胞室中受体和离子通道的密度和功能耦合,以及它们相对于兴奋性和抑制性突触位点的位置。因此,如何在高分辨率下确定这些分子的精确亚细胞位置的问题就出现了。
先进的高分辨率免疫细胞化学方法
为此目的,以下先进的高分辨率免疫细胞化学方法已被广泛应用:(i)预包埋免疫金,(ii)包埋免疫金,(iii)十二烷基硫酸钠(SDS)-消化冷冻骨折复制标记(SDS- frl)技术。(i)在预包埋免疫金方法中,将0.8 nm或1.4 nm的金粒子偶联到第二抗体上,以促进适当的穿透。随后对金粒子进行银强化以产生可检测的粒子大小。
这种方法产生非扩散标签,从而可以确定反应的精确位置和蛋白在突触外和突触周围的位置。然而,使用这种方法无法检测到突触蛋白,最可能的原因是固定组织的突触特化中无法获得表位[2].(ii)包埋后免疫金方法通过免疫化学试剂与暴露在超薄切片表面的抗原反应,以与非突触分子同样的灵敏度检测突触蛋白,克服了预包埋技术的问题。这也提高了蛋白质密度的定量评价。
然而,在树脂包埋的切片中,大量蛋白质被埋,因此抗体无法获取,限制了该技术的检测灵敏度[2].(iii)在SDS-FRL中,脑组织用高压冷冻机冷冻(徕卡EM HPM100),然后将冷冻样本放入复制机(徕卡em baf060).蛋白质被分配到质膜的原质面(p面)或外质面(e面)。分子被一层薄的碳(3-5纳米)固定,然后进一步涂上一层2纳米厚的铂/碳层来遮蔽膜面,然后用15-20纳米厚的碳沉积来加强这种材料[3.].与传统的免疫功能相比,SDS-FRL技术具有两个主要优点。
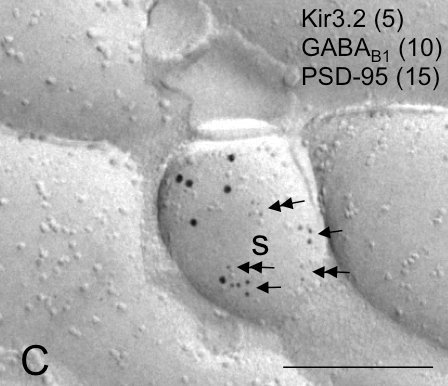
首先,SDS-FRL的敏感性远远高于包埋前和包埋后技术,因为膜蛋白暴露在复制体的二维表面上(图1),使它们易于获得免疫试剂。此外,表位通过SDS变性,使已知适合免疫印迹分析的抗体与固定在复制膜上的蛋白质发生类似的反应。第二,可以同时可视化突触和突触外蛋白,实现膜段免疫金密度的定量。
参考
- 抑制主题的变化:GABA(A)受体的阶段性和紧张性激活。自然Rev神经科学6:3(2005)215-229。
- Lujan R, Nusser Z, Roberts JDB, Shigemoto R, Somogyi P: mGluR1和mGluR5在大鼠树突和树突棘上的突触周围位置。欧洲神经科学杂志8:7(1996)1488-1500。
- Fukazawa Y, Masugi-Tokita M, Tarusawa E, Hagiwara H, Shigemoto R: SDS-FRL -消化冷冻骨折复制标记(SDS-FRL), in: Handbook of cryogenic preparation Methods for Electron microscopy, eds。Cavalier A, Spehner D, Humbel BM;CRC出版社,纽约(2009)567-586。
- Kulik A, Vida I, Fukazawa Y, Guetg N, Kasugai Y, Marker CL, Rigato F, Bettler B, Wickman K, Frotscher M, Shigemoto R.在海马锥体细胞中,包含kir3.2的K+通道和GABAB受体的区段依赖性共定位。神经科学杂志26:16(2006)4289-4297。
- Masugi-Tokita M, Tarusawa E, Watanabe M, Molnar E, Fujimoto K, Shigemoto R: sds -消化冷冻骨折复制标记揭示的大鼠小脑突触AMPA受体的数量和密度。神经科学学报27:8 (2007a) 2135-2144。
- Masugi-Tokita M, Shigemoto R:中央突触谷氨酸和GABA受体的高分辨率定量可视化。神经生物学当前观点17 (2007b) 387-393。
- Fujimoto K:冷冻断裂复制电镜结合SDS消化用于细胞化学标记完整的膜蛋白。细胞科学杂志108(1995)3443-3449。