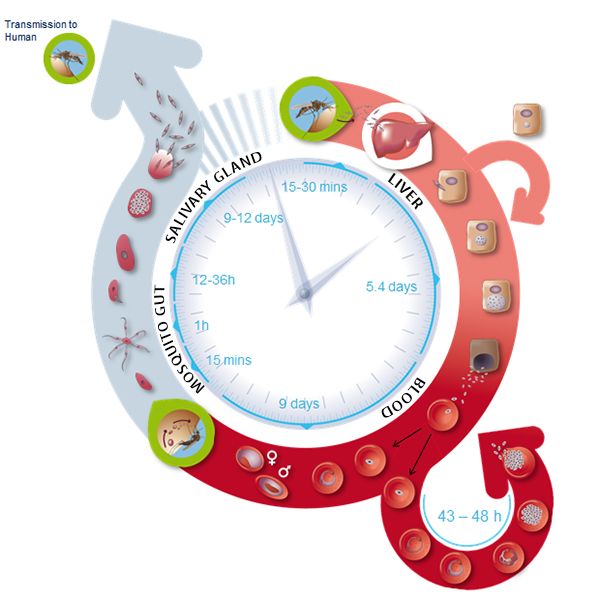
了解疟疾感染的关键球员
进入人类宿主后,疟原虫寄生虫在其生命周期中以不同的形式存在,因为疟疾发展(图1)。在所谓的血液阶段[3], 这Merozoite.形式侵入红细胞(红细胞),通过不同的阶段演变,并产生大约30个女儿的Merozoites,从被感染的宿主细胞中出现,准备攻击其他细胞。MEROZOITE入侵是血液中寄生虫在血液和发作的关键。尽管如此,疾病的分子机制仍然不清楚。
要侵入红细胞,Menozoite形式必须首先与宿主细胞接触,所谓的“前进”相188金宝搏的网址[4]。初始相互作用使红细胞膜变形,Merozoite配体与膜中的特异性受体结合以产生紧密的连接,以及CA2+触发离子磁通。加利福尼亚州2+Flux似乎对细胞入侵很重要。对细胞的寄生虫附着变得不可逆,并且在不到2分钟内进入红细胞。
P. falciparum.网状细胞结合蛋白质同源物(PFRH)和红细胞结合样蛋白是信号传导侵袭的重要参与者[5]。PFRH系列的关键构件是PFRH5,其与宿主蛋白受体Basigin结合。这种交互引起CA2+释放到红细胞中并表明孔桥接混血素和血细胞膜的形成。PFRH5对于Merozoite入侵是必不可少的,如研究所示,其中抗体或可溶性碱抑制红细胞感染[6]。PDRH5与PFRH5相互作用蛋白(PFRIPR)和富含半胱氨酸的保护性抗原(Cyrpa)一起工作,但这种相互作用的功能方面是未知的。理解PFRH5 / PFRIPR / Cyrpa的作用重要性,因为这些蛋白质是开发疫苗的疫苗患有疫苗,抑制血液阶段的疟疾进展[7]。
用合适的工具找到疟疾感染的答案
用纸纳米透视放大
接下来,墨尔本研究人员在入侵期间调查了PFRH5,PFRIPR和Cyrpa的定位[2]。共聚焦成像揭示了寄生虫顶端的三种蛋白质的优先定位,该区域优先与宿主细胞接触。188金宝搏的网址然而,只有能够将细节溶解在衍射极限下方的细节≥通常低于30nm和100nm的衍射极限的纳米镜的纳米镜,仅可以进行精确评估生物分子的空间分布。st(刺激排放耗尽)。为此,将红细胞与Merozoites一起温育以诱导侵袭并用抗靶蛋白的抗体标记。用2D和3D安装并成像样品st纳米镜。为了进一步鉴定侵袭的初始阶段,免疫荧光标记包括对RON4的标记物,在寄生虫的顶端定位蛋白质(图2)。
使用的空间信息st展示了PFRH5,PFRIPR和Cyrpa的共定位,在顶端,RON4也存在。单个蛋白质和二分PFRH5 / PFRIPR和Cyrpa / PFRIPR络合物显示出在Merozoite膜上的拼接分布,与顶端释放一致。与2D更近的,更高的分辨率评估st证实,PFRIPR和Cyrpa在Merozoite上铺展,但特别是在顶端局部定位。估计PFRH5 / PFRIPR和CyrPA / PFRIPR的共同定位程度显示出较大比例的PFRH5 / PFRIPR。该发现表明,Cyrpa / PFRIPR将PFRH5 / Cyrpa / PFRIPR复合物直接组装在表面顶端以进行结合Basigin。此事件触发了紧密交界处的形成,并启用下一个侵入步骤。单独的PFRH5,PFRIPR和Cyrpa信号的存在还表明每种蛋白质的显着池仍然可用于复杂的形成。
外表
红细胞侵袭是人类宿主疟疾感染的关键阶段。直到最近,涉及所涉及的蛋白质的相互作用和功能的研究受到限制,因为抑制关键配体PFRH5抑制侵袭。Cowman集团利用PFRIPR和Cyrpa的条件表达揭示了PRIPR,Cyrpa和PFRH5 / PFRIPR / Cyrpa综合体在Merozoite入侵中的基本作用[2]。蛋白质参加了加利福尼亚州2+通过形成和结合到宿主受体Basigin的形成和结合释放到红细胞中。st纳米镜提供必要的分辨率,以显示PFRH5 / PFRIPR / Cyrpa在寄生虫和宿主细胞之间的界面处形成。以前的研究表明,Cyrpa将复合物与寄生虫膜联系起来[8],但Cowman组进行了额外的生化测定,表明这不是这种情况。相反,结果表明,其他蛋白质必须将复合物锚定到宿主细胞并将其引导在顶端形成。
未来的工作将有助于找到参与Merozoite /宿主细胞互动的新型蛋白质,了解CA的功能作用2+在感染途径中释放。最终,解剖宿主和病原体之间的相互作用将有助于寻找更有效的疟疾抗击疟疾方式。
参考
- 世界卫生组织(世卫组织),2017年世界疟疾报告(世卫组织,瑞士日内瓦,2017年11月29日)
- Volz, J.C., Yap, A., Sisquella, X., Thompson, J.K., Lim, N.T., Whitehead, L.W., Chen, L., Lampe, M., Tham, W.H., Wilson, D., Nebl, T., Marapana, D., Triglia, T., Wong, W., Rogers, K.L., Cowman, A.F. Essential Role of the PfRh5/PfRipr/CyRPA Complex during疟原虫疟原虫侵袭红细胞,细胞宿主微生物。(2016年7月13日)20(1),60-71,DOI:10.1016 / J.Chom.2016.06.004
- Cowman,A.F.,Crabb,B.S.通过疟疾寄生虫侵袭红细胞,细胞(2006)124,755-766,DOI:10.1016 / J.Cell.2006.02.006
- Weiss,G.E.Gilson,P.R.,Taechalertpaisarn,T.,Tham,W.-H.,De Jong,N.w.m.,Harvey,K.L.,Fowkes,F.J.I.,Barlow,P.N.,Rayner,J.C.,Wright,G.J.,Cowman,A.F.,Crabb,B.S.揭示受体 - 配体相互作用的序列并得到的细胞形态疟原虫疟原虫侵袭红细胞。PLOS POAROG。(2015)11(2),E1004670,DOI:10.1371 / journal.ppat.1004670
- Tham,W.H.,治疗师,J.,Cowman,A.f.红细胞和网状细胞结合样蛋白疟原虫疟原虫。趋势寄生醇。(2012)28(1),23-30,DOI:10.1016 / J.PT.2011.10.002
- Chen, L., Lopaticki, S., Riglar, D.T., Dekiwadia, C., Uboldi, A.D., Tham, W.-H., O'Neill, M.T., Richard, D., Baum, J., Ralph, S.A., Cowman, A.F. An EGF-like protein forms a complex with PfRh5 and is required for invasion of human erythrocytes by疟原虫疟原虫。PLOS POAROG。(2011)7(9),E1002199,DOI:10.1371 / journal.ppat.1002199
- Douglas, A.D., Baldeviano, G.C., Lucas C.M., Lugo-Roman L.A., Crosnier C., Bartholdson S.J., Diouf A., Miura K., Lambert L.E., Ventocilla J.A., Leiva K.P., Milne K.H., Illingworth J.J., Spencer A.J., Hjerrild K.A., Alanine D.G., Turner A.V., Moorhead J.T., Edgel K.A., Wu Y., Long C.A., Wright G.J., Lescano A.G., Draper S.J. A PfRH5-based vaccine is efficacious against heterologous strain blood-stage疟原虫疟原虫感染AOTUS.猴子,细胞主体微生物(2015)17(1),130-139,DOI:10.1016 / J.Chom.2014.11.017
- reddy,K.S.Amlabu E.,Pandey A.K.,Mitra P.,Chauhan V.S.,Gaur D.用PFRH5和PFRIPR与PFRH5和PFRIPR之间的Multi incotin复合物对其至关重要疟原虫疟原虫红细胞侵入,proc。Natl。阿卡。SCI。美国(2015)112(4),1179-1184,DOI:10.1073 / PNAS.1415466112